27 czerwca 2024
Nanocząstki złota zabijają nowotwory – ale nie tak, jak myślano
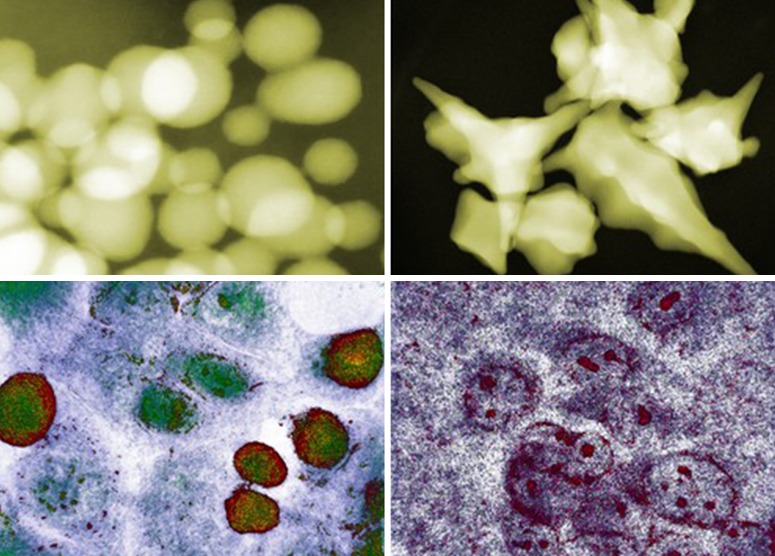
Naukowcy z Instytutu Fizyki Jądrowej PAN w Krakowie odkryli, że nanocząstki złota, choć znane ze swojej zdolności do zabijania komórek nowotworowych, działają w sposób bardziej złożony niż wcześniej sądzono. Dotychczas uważano, że mniejsze nanocząstki są bardziej skuteczne, ponieważ łatwiej wnikają do wnętrza komórek rakowych, prowadząc do ich śmierci. Jednak badania wykazały, że większe, gwiaździste nanocząstki o rozmiarze 200 nanometrów są bardziej toksyczne dla komórek glejaka niż mniejsze, sferyczne nanocząstki o rozmiarze 10 nanometrów.
Komórka pod obserwacją w naturalnym środowisku
Dr hab. inż. Joanna Depciuch-Czarny, inicjatorka badań, podkreśla, że odkrycie to było możliwe dzięki zastosowaniu nowatorskiej techniki mikroskopii holotomograficznej. Mikroskop ten, pierwszy w Polsce, pozwala na obserwację komórek w ich naturalnym środowisku bez konieczności wprowadzania obcych substancji. Dzięki temu naukowcy mogli dokładnie prześledzić interakcje nanocząstek złota z komórkami nowotworowymi w czasie rzeczywistym.
Unikatowe cechy holotomografii w badaniach nad nanocząstkami złota
Krakowscy fizycy z Instytutu Fizyki Jądrowej PAN odkryli przyczyny nieoczekiwanych zachowań komórek nowotworowych w obecności nanocząstek złota. Badania przeprowadzono na trzech liniach komórkowych: dwóch glejaka i jednej jelita grubego. Małe, sferyczne nanocząstki łatwo wnikały do wnętrza komórek rakowych, które mimo początkowego stresu regenerowały się i ponownie dzieliły. Natomiast duże, gwiaździste nanocząstki dziurawiły błony komórkowe, co prowadziło do stresu oksydacyjnego i apoptozy.
Dr hab. Paweł Jakubczyk z Uniwersytetu Rzeszowskiego, współtwórca modelu teoretycznego, podkreśla, że model ten pozwala na szybkie ustalenie absorpcji nanocząstek przez komórki nowotworowe. Dzięki temu można zredukować liczbę eksperymentów, obniżając koszty i skracając czas badań. Model ten może również pomóc w projektowaniu celowanych terapii, minimalizując toksyczność wobec zdrowych komórek.
Grupa naukowców planuje kontynuować badania, rozszerzając model o dodatkowe parametry, takie jak skład chemiczny nanocząstek i różne rodzaje nowotworów. W przyszłości planowane jest również optymalizowanie efektywności terapii fotonowej i protonowej. Badania te otwierają nowe możliwości w terapii nowotworowej, wskazując na konieczność dalszych badań nad różnymi kształtami i rozmiarami nanocząstek, aby lepiej zrozumieć ich działanie i zoptymalizować ich wykorzystanie w medycynie.
Więcej w materiale: Serwis prasowy IFJ PAN
- (Źródło: IFJ PAN)
- (Źródło: IFJ PAN)